教育经历:
2005 – 2010, 理学博士,芝加哥大学化学系
2001 – 2005, 理学学士,中国科学技术大学化学系
工作经历:
2019- 至今,正教授,6165cc金沙总站检测中心
2014 - 至今,研究员(双聘),北京大学化学与分子工程学院
2013 - 至今,研究员,北京大学合成与功能生物分子中心
2012 - 至今,研究员,北大清华生命联合中心
2017 - 2018,长聘副教授,6165cc金沙总站检测中心
2012 - 2017,助理教授,6165cc金沙总站检测中心
2010 – 2011,博士后,芝加哥大学生物化学与分子生物学系
荣誉奖励:
第八届中国化学会-英国皇家学会青年化学奖,2022
茅以升北京青年科技奖,2022
中源协和生命医学奖创新突破奖,2022
国家自然科学基金委杰出青年科学基金项目,2018
科技部中青年科技创新领军人才,2018
OKeanos-CAPA Young Investigator Award,2018
Bayer Investigator Award at PKU,2018
中国化学会化学生物学奖突出贡献奖(35周岁以下),2018
第十六届霍英东青年教师基金,2018
第十届“药明康德生命化学研究奖”学者奖,2016
中国化学会青年化学奖,2016
国家自然科学基金委优秀青年科学基金项目,2015
IUPAC Prize for Young Chemists, 2011
学术任职:
2017 - present, the Chinese Cell Biology Society
2013 – present, the RNA society
2013 – present, the Chinese Society of Biochemistry and Molecular Biology
2012 – present, the Chinese Crystallographic Society
2012 – present, the Chinese Chemical Society
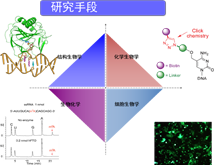
实验室致力于RNA/DNA修饰的生物学通路、功能和机制研究以及基因编辑新方法的开发。为了实现这一目标,我们综合运用包括化学生物学、表观遗传学、基因编辑、单细胞组学和基因组学等多学科手段,旨在揭示核酸表观遗传修饰的新颖功能和调控机制。
1. RNA修饰和表观转录组学
几十年的研究已经鉴定了100多种转录后修饰。研究人员之前认为,一旦RNA修饰产生,这些共价修饰都是稳定存在、不可逆转的。然而,最近关于6-甲基腺嘌呤(m6A)的一系列研究证明,RNA甲基化也是动态可逆的,并且在基因表达调控中起到重要作用。因此,“表观转录组学”也随之兴起。
除了m6A,转录组上还存在其它表观遗传修饰。我们课题组最近的研究发现,多种之前认为只在非编码RNA上存在的转录后修饰,即假尿嘧啶(Ψ)和1-甲基腺嘌呤(m1A),也广泛存在于哺乳动物的mRNA当中。我们的研究表明这些转录后修饰在转录组中广泛存在,受多种外界刺激的动态调控,并且对于m1A来说,可以被潜在的“eraser”消码器蛋白去甲基化。然而,mRNA上m1A和Ψ修饰的生物学功能还尚不清楚。此外,我们最近鉴定了mRNA上的动态、可逆修饰m6Am。我们希望利用课题组已经开发的新颖表观转录组测序技术,来阐释这些RNA修饰在生理及病理条件下的功能和调控机制,从而在表观转录组学这个新兴起的学科中发现一片“新大陆”。
2. 基因编辑
基因编辑作为新兴的颠覆式生物技术,已经在生物医药、农业、能源和生物安全等方面展现了巨大的潜力。基于我们在化学生物学、分子生物学和高通量测序等方面的特长,本课题组也评价现有的基因编辑工具,并发展更为精准、强大、便捷的基因编辑新技术。
3. DNA修饰和表观基因组学
哺乳动物基因组中,具有5-甲基胞嘧啶(5mC)、5-羟甲基胞嘧啶(5hmC)、5-醛基胞嘧啶(5fC)和5-羧基胞嘧啶(5caC)等多种表观基因组修饰。本实验室开发了多个单碱基、单细胞水平上表观基因组的组学检测技术,未来将应用于单细胞测序和临床研究,以期鉴定疾病的生物标志物。此外,我们也关注染色质可及性的组学检测技术。
1. Song J, Dong L, Sun H, Luo N, Huang Q, Li K, Shen X, Jiang Z, Lv Z, Peng L, Zhang M, Wang K, Liu K, Hong J, Yi C. CRISPR-free, programmable RNA pseudouridylation to suppress premature termination codons. Mol Cell. 2023, 83, 139-155.
2. Liu C, Sun H, Yi Y, Shen W, Li K, Xiao Y, Li F, Li Y, Hou Y, Lu B, Liu W, Meng H, Peng J, Yi C *, Wang J.* Absolute quantification of single-base m6A methylation in the mammalian transcriptome using GLORI. Nat Biotechnol. 2023,41,355-366.
3. Zhang M, Jiang Z, Ma Y, Liu W, Zhuang Y, Lu B, Li K, Peng J, Yi C*. Quantitative profiling of pseudouridylation landscape in the human transcriptome. Nat Chem Biol. 2023 Mar 30. doi: 10.1038/s41589-023-01304-7.
4. Lei Z, Meng H, Liu L, Zhao H, Rao X, Yan Y, Wu H, Liu M, He A,Yi, C*. Mitochondrial base editor induces substantial nuclear off-target mutations. Nature. 2022,606, 804–811
5. Chen L, Zhu B, Ru G, Meng H, Yan Y, Hong M, Zhang D., Luan C, Zhang S., Wu H., Gao H, Bai S, Li C, Ding R, Xue N, Lei Z, Chen Y, Guan Y, Siwko S, Cheng Y, Song G, Wang L, Yi C*, Liu M*, Li D* Re-engineering the adenine deaminase TadA-8e for efficient and specific CRISPR-based cytosine base editing. Nat Biotechnol. 2022, Nov 10. doi: 10.1038/s41587-022-01532-7
6. Zhuang Y, Liu J, Wu H, Zhu Q, Yan Y, Meng H, Chen PR, Yi C*. Increasing the efficiency and precision of prime editing with guide RNA pairs. Nat Chem Biol. 2022; 18:29-37.
7. Lei Z, Meng H, Lv Z, Liu M, Zhao H, Wu H, Zhang X, Liu L, Zhuang Y, Yin K, Yan Y, Yi C.* Detect-seq reveals out-of-protospacer editing and target-strand editing by cytosine base editors. Nat Methods. 2021; 18:643-651.
8. Cui Q, Yin K, Zhang X, Ye P, Chen X, Chao J, Meng H, Wei J, Roeth D, Li L, Qin Y, Sun G, Zhang M, Klein J, Huynhle M, Wang C, Zhang L, Badie B, Kalkum M, He C, Yi C* and Shi Y*. Targeting PUS7 suppresses tRNA pseudouridylation and glioblastoma tumorigenesis. Nat Cancer.2021; 2:932–949.
9. Liu J, Li K, Cai J, Zhang M, Zhang X, Xiong X, Meng H, Xu X, Huang Z, Peng J. Fan J*, YI C*. Landscape and Regulation of m6A and m6Am Methylome across Human and Mouse Tissues. Mol Cell. 2020; 77:426-440.
10. Song J, Zhuang Y, Zhu C, Meng H, Lu B, Xie B, Peng J, Li M*, Yi C*. Differential roles of human PUS10 in miRNA processing and tRNA pseudouridylation. Nat Chem Biol. 2020; 16: 160-169.
实验室致力于RNA/DNA修饰的新生物学通路、新功能和新机制研究以及基因编辑新方法的开发。我们综合运用包括化学生物学、表观遗传学、RNA修饰、基因编辑、单细胞组和基因组学等多学科手段,尤其关注RNA生物学在人类疾病诊断与治疗当中的应用。

实验室电话8610-62752895
 下载Firefox
下载Firefox
 下载Firefox
下载Firefox



 下载Firefox
下载Firefox